سیستم تعادلی اکسیژن – آهن
اگر آهن مذاب را در تماس با اکسیژن قرار دهیم در دماهاي مختلف اکسیژن در آن حل میشود. میزان حلالیت آهن در اکسیژن بستگی به دما دارد. اگر میزان اکسیژن موجود در مذاب از حد حلالیت آن بیشتر شود باعث بوجود آمدن اکسید آهن میشود. شکل زیرحلالیت اکسیژن را در آهن در دماهاي مختلف نشان می دهد.

حلالیت اکسیژن در آهن با تغییر دما
با افزایش دما حد حلالیت زیاد می شود لذا در فولادسازي که دما بالا است باید زمان را کم کنیم تا اکسیژن کمتري حل شود و یا اینکه شرایط انحلال آهن را محدود کنیم. مثلا از سرباره هاي شامل SiO2 و CaO استفاده کنیم. این سرباره ها میزان انحلال اکسیژن در فولاد را کم می کنند چون بر روي ضریب اکتیویته اکسیژن در مذاب تاثیر میگذارند. یا اینکه باعث می شوند FeO اجازه آزاد کردن اکسیژن را نداشته و اکسیژن را به مذاب بر نگرداند.
(FeO)=[Fe]+[O]

تاثیر فشار اکسیژن بر انحلال آن
در این شکل تاثیر فشار اکسیژن بر میزان اکسیژن حل شده نشان داده میشود. نمودارها بر اساس محاسبات ترمودینامیکی زیر رسم شده اند.
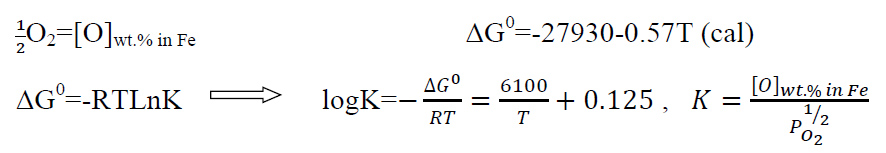
ΔG برحسب استاندارد یک درصد وزنی است.
استاندارد یک درصد وزنی: ابتدا فشار بخار جسم خالص A را اندازه گیري میکنند سپس به آن یک درصد وزنی از ماده B اضافه میکنند. دوباره فشار بخار را اندازه می گیرند و نسبت این دو فشار بخار اکتیویته یک درصد وزنی را نشان می دهد. با افزایش فشار اکسیژن، میزان اکسیژن حل شده در مذاب زیاد میشود تا به حد اشباع اکسیژن در آن دما برسد. در دماهاي مختلف حد اشباع اکسیژن فرق می کند. با گذشتن از حد اشباع آهن اکسید می شود.
» نوشته مرتبط: قیمت تیرآهن
سیستم هاي پیچیده مانند Fe-a-b-c
اثر عوامل مختلف را بر ضرایب اکتیویته بررسی می کنند، مثلا ![]()
براي حل آن از بسط لاگرانژ استفاده می شود:
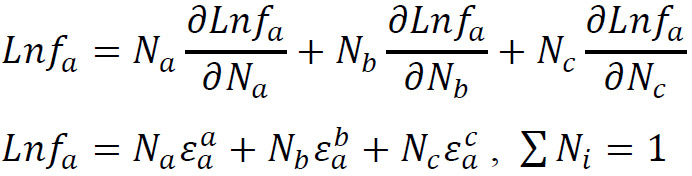
𝜀aa ضریب تاثیر متقابل جزء a بر روي خودش
𝜀ba ضریب تاثیر متقابل جزء b بر روي جزء a
روش دیگر نمایش :
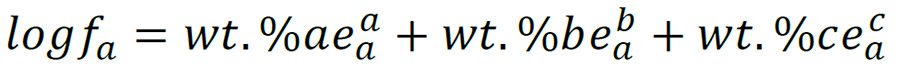
براي مطالعه سیستم هاي خیلی پیچیده آنها را به سیستم هاي کوچکتر می شکنیم (همیشه سیستمهاي 2 و سه تایی را مطالعه می کنیم.). دو شکل زیر اثر عناصر آلیاژي را بر روي ضریب اکتیویته گوگرد در آهن در 1600 درجه سانتیگراد نشان می دهند.
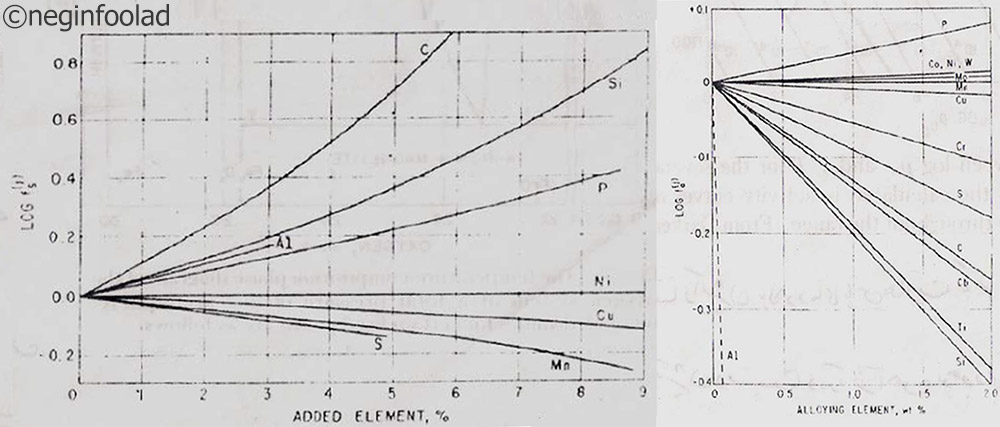
عناصر آلیاژی بر روی ضریب اکتیویته گوگرد
سیستم تعادلی آهن-کربن-اکسیژن
کربن زدایی آلیاژ مذاب Fe-C توسط اکسیژن گازي که درون حمام دمیده میشود و یا توسط کانی آهن شارژ شده انجام میگیرد. ابتدا اکسیژن طبق واکنشهاي زیر در مذاب حل می شود.
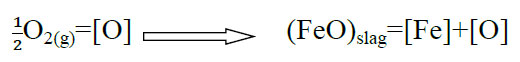
اکسیژن حل شده طبق واکنشهاي زیر با کربن واکنش می دهد.

محصول اصلی واکنش مونوکسید کربن است اما مقداري CO2 نیز تولید خواهد شد.
براي واکنش تولید مونوکسید کربن داریم:
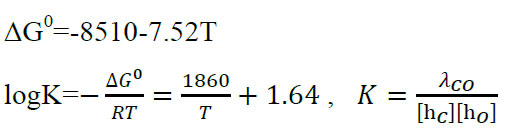
که در آن H و Hc اکتیویته هاي هنرین اکسیژن و کربن هستند. 𝜆co فشار جزئی گاز CO میباشد. اگر رفتار محلول رقیق در نظر گرفته شود رابطه بالا به صورت زیر نوشته خواهد شد:
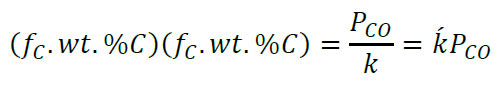
این رابطه، ارتباط معکوس اکسیژن و کربن موجود در آهن مذاب را نشان میدهد. همچنین میتوان اینگونه نتیجه گرفت که انحلال اکسیژن در حمام Fe-C با افزایش فشار جزئی CO افزایش خواهد یافت و برعکس (کاهش فشار CO با دمش گاز خنثی یا با ایجاد خلاء بدست می آید.) در شرایط عملی فشار جزئی گاز CO بین 1.1 تا 1.3 اتمسفر میباشد. نتایج آزمایشگاهی Chipman و همکارانش این پدیده را نشان می دهد.
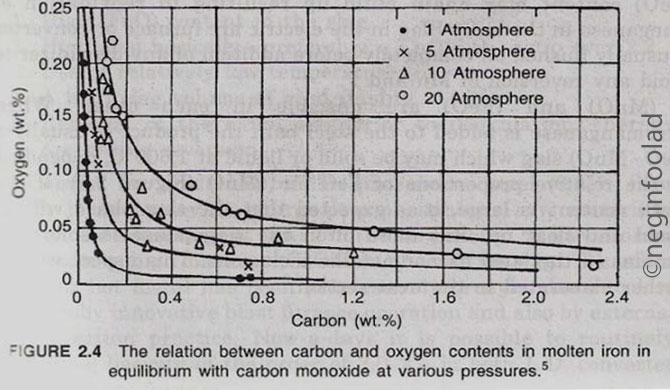
رابطه اکسیژن و کربن با فشار
ضریب اکتیویته کربن در آهن آلات مذاب نیز تابعی از محتواي کربن است. این اثر توسط شکل زیر براي تغییرات ضریب اکتیویته کربن در محلول آهن در دماي 1600 درجه سانتیگراد به عنوان تابعی از ترکیب شیمیایی در یک محلول بسیار رقیق نشان داده می شود.
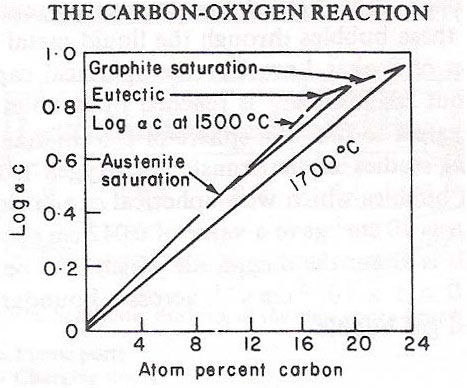
واکنش کربن و اکسیژن
شکل زیر تغییرات حاصلضرب غلظت کربن و اکسیژن را در فشار یک اتمسفر CO+CO2 نشان میدهد. بسیار جالب است که مشخص شود که فرآیند تصفیه چقدر نزدیک به شرایط ترمودینامیکی می باشد.
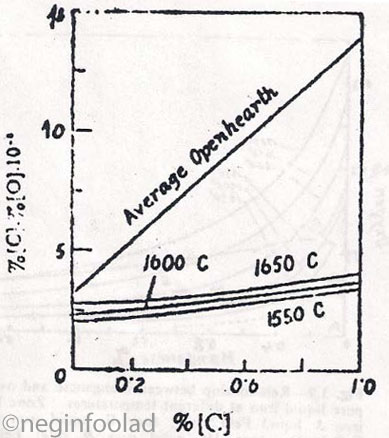
غلظت کربن و اکسیژن در فشار یک اتمسفر
در یک [C] ثابت با افزایش دما حاصلضرب [C][O] بیشتر میشود. یعنی اکسیژن و کربن بیشتري در فولاد حل میشود. در خط بالایی هم حالت واقعی کوره زیمنس مارتین دیده میشود. مشخص است که حاصلضرب محتواي کربن و اکسیژن اندازه گیري شده در حین فرآیند تصفیه در کوره اجاق باز قلیایی بسیار از مقادیر تعادلی در فشار یک اتمسفر CO دور است. اگر این شکل را با شکل زیر (که باز براي اجاق باز است) مقایسه کنیم مشخص است که درصد اکسیژن با مقدار محاسبه شده از نظر تئوري در کنورتر اجاق باز همخوانی خوبی نشان میدهد لذا مشخص میشود که میزان انحلال کربن در کوره اجاق باز خیلی بیشتر از مقدار تعادلی است.
- منبع: به نقل از دکتر مهدی مزمل / دانشگاه صنعتی سهند







